Actualizado 09 junio 2023
Definición
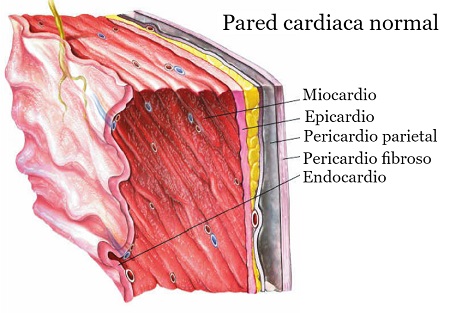
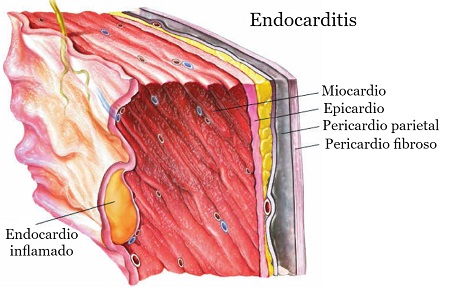
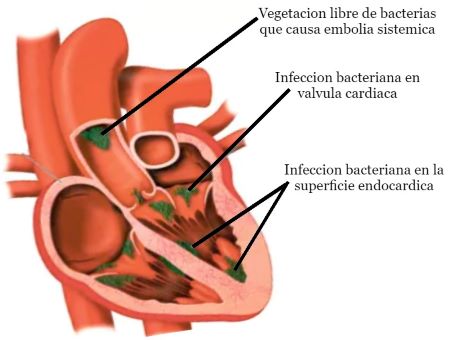
Infección del endocardio, siendo las válvulas cardíacas las estructuras más comúnmente afectadas.
Etiología
Principales etiologías (en orden de frecuencia): Actualmente se acepta que, en general, Staphylococcus aureus es la principal causa de endocarditis infecciosa (EI):
- EI subaguda en válvula nativa: Streptococcus viridans, enterococos.
- EI válvula nativa aguda: Staphylococcus aureus, Streptococcus pneumoniae.
- EI precoz en válvula protésica: Estafilococos coagulasa negativos, S. aureus, bacilos gramnegativos, enterococos, hongos.
- EI intermedia en válvula protésica: Estafilococos coagulasa negativos, enterococos, S. aureus, hongos, estreptococos.
- EI tardía en válvula protésica: Streptococcus viridans, S. aureus, estafilococos coagulasa negativos, enterococos.
- Otros microorganismos: Coxiella, bartonella, grupo HACEK (Haemophilus, Actinobacillus, Eikenella, Kingella).
Presentación clínica
Cuadro clínico: Cuadro más exuberante en endocarditis aguda y más prolongado en endocarditis subaguda:
- Síndrome febril: Fiebre con escalofríos y sudoración asociada.
- Soplo cardíaco: Nuevos soplos o cambios en soplos previos, especialmente en el cuadro agudo, que pueden estar presentes hasta en el 85% de los casos.
- Esplenomegalia: Principalmente en la forma subaguda.
- Fenómenos embólicos: Petequias, nódulos de Osler (poco comunes en la era posterior a los antibióticos), lesiones de Janeway, hemorragia intracraneal, embolia séptica, manchas en astilla (hemorragias subungueales).
- Fenómenos inmunológicos: Poliartralgia, manchas de Roth, glomerulonefritis, dedos en palillos de tambor, nódulos de Osler.
- Síntomas inespecíficos: Disnea, malestar general, cefalea, mialgias, pérdida de peso, anorexia, sudores nocturnos, tos, dolor abdominal, dolor torácico de tipo pleurítico.
Asociaciones comunes
- Endocarditis en usuario de drogas EV (pp. en válvula tricúspide): Staphylococcus aureus, Pseudomonas aeruginosa, cándida.
- Endocarditis por enterococos: Relación con manipulación del tracto genitourinario.
- Endocarditis por Streptococcus bovis: Relación con malignidad del tracto gastrointestinal y pólipos colónicos (colonoscopia indicada).
- Endocarditis con hemocultivos negativos: Grupo HACEK (Haemophilus, Actinobacillus, Cardiobacterium hominis, Eikenella corrodens, Kingella kingae). Pueden tardar entre 14 y 21 días en crecer en medio de cultivo.
Factores de riesgo
- Uso de drogas intravenosas (S. aureus).
- Prótesis valvular, incluyendo TAVI (principal factor de riesgo individual).
- Cardiopatía estructural (lesión reumática, prolapso de la válvula mitral, cardiopatías congénitas, hipertrofia del tabique interventricular, coartación aórtica).
- Inmunosupresión e infección por VIH.
- Endocarditis previa.
- Presencia de dispositivos intravasculares.
- Dispositivos cardíacos implantables.
- Edad mayor de 60 años.
- Mala higiene dental.
- Hemodiálisis de larga data.
- Masculino.
Enfoque diagnóstico
El diagnóstico involucra criterios clínicos, de laboratorio y de ecocardiograma. El diagnóstico se puede cerrar según los criterios de Duke.
Exámenes de laboratorio de rutina:
Hemograma completo, creatinina, urea, creatinina, electrolitos, glucosa, coagulograma, VHS y PCR, electrocardiograma y radiografía de tórax.
Hemocultivos:
Un mínimo de tres pares de cultivos, dos muestras de diferentes sitios, con un intervalo de una hora entre los pares. Cada par consta de un tubo para aeróbicos y uno para anaeróbicos, con 10 ml de sangre venosa en cada uno. Se debe informar al laboratorio sobre la posibilidad de un germen de crecimiento lento.
Ecocardiograma:
Siempre está indicado ante la sospecha de endocarditis. En pacientes con válvula nativa se opta por el ecocardiograma transtorácico (ETT), reservando el ecocardiograma transesofágico (ETE) para casos de duda diagnóstica (ETT no concluyente o negativo en un paciente con alta sospecha clínica), cuadros graves con sospecha de complicaciones o con empeoramiento clínico.
Cuando el ETE es negativo y el paciente sigue teniendo EI como principal hipótesis diagnóstica, se debe solicitar un segundo examen en 2-7 días, buscando evidenciar la presencia de vegetación. Un segundo examen negativo hace que esta hipótesis sea poco probable.
Tomografía computarizada:
Prueba ideal para detectar complicaciones como absceso aórtico o paravalvular y aneurisma micótico (angiotomografía). También puede utilizarse para detectar complicaciones embólicas cuando se sospeche de ellas con base en la historia clínica y el examen físico.
No debe utilizarse como herramienta diagnóstica, ya que no ha demostrado mejorar significativamente el diagnóstico y ha aumentado la incidencia de nefropatía por contraste.
PET/TC-FDG:
Examen que detecta la actividad inflamatoria a través del consumo de energía de las células, pero no puede distinguir la infección de la inflamación. Por lo tanto, es menos útil en válvulas protésicas en el post-operatorio temprano.
Gammagrafía con leucocitos marcados:
Es el principal método en pacientes con dispositivos implantados, como DAI, con una sensibilidad del 90% y una especificidad del 100%.
Criterios de Duke
Diagnóstico de endocarditis: Presencia de dos criterios mayores, uno mayor y tres menores, o cinco criterios menores.
El diagnóstico definitivo también puede establecerse mediante examen anatomopatológico o cultivos de materiales o válvulas extraídas durante la cirugía.
Posible diagnóstico: Presencia de un criterio mayor y uno o dos menores, o entre tres y cuatro criterios menores.
Criterios mayores:
- Hemocultivo: Dos muestras positivas para el organismo típico (ver etiología arriba); o bacteriemia persistente con organismo consistente (en dos muestras con más de 12 horas de diferencia; tres muestras todas positivas; cuatro o más muestras en su mayoría positivas); o muestra única positiva para Coxiella burnetii o título de anticuerpo antifase I IgG > 1:800.
- Ecocardiograma: Presencia de vegetación, absceso, dehiscencia parcial de la válvula protésica o insuficiencia valvular nueva compatible con endocarditis infecciosa (también se puede considerar la presencia de un nuevo soplo a la exploración, pero no basta con el empeoramiento de un soplo antiguo).
Criterios menores:
- Factor de alto riesgo: Usuario de drogas intravenosas y cardiopatía estructural.
- Fiebre ≥ 38°C.
- Fenómenos embólicos: Embolismo pulmonar periférico o séptico, hemorragia intracraneal, hemorragias subconjuntivales, lesiones de Janeway, y aneurismas micóticos.
- Fenómenos inmunológicos: Poliartralgia, manchas de Roth, glomerulonefritis, dedos en palillo de tambor, y los nódulos de Osler.
- Evidencia microbiológica que no cumple con los criterios mayores: Hemocultivos positivos o evidencia serológica de endocarditis.
Endocarditis con hemocultivos negativos: Cuando la sospecha diagnóstica es alta y los cultivos permanecen negativos, se deben considerar algunas posibilidades, como microorganismos de crecimiento lento, microorganismos exigentes en relación con los medios de cultivo o incluso intracelulares, que pueden detectarse mediante serología o reacción en cadena de polimerasa. Otra causa importante de cultivos negativos es el uso de antibióticos antes de la recolección de cultivos.
Clasificación
Es posible clasificar las endocarditis en válvulas nativas según su duración y evolución. Las endocarditis en válvulas protésicas, por su parte, se clasifican en función del tiempo de aparición desde la colocación de la prótesis:
- Válvula nativa aguda: Duración < 6 semanas. Se presenta desde el inicio con importante toxicidad, evolucionando rápidamente a destrucción valvular e infección metastásica. Principal agente etiológico: Staphylococcus aureus.
- Válvula nativa subaguda: Duración > 6 semanas. Evoluciona insidiosamente durante semanas a meses, con toxicidad leve y raras manifestaciones sistémicas. Principales agentes etiológicos: Streptococcus viridans, enterococos, estafilococos coagulasa negativos y bacilos gramnegativos.
- Prótesis valvular temprana: Aparece en menos de 2 meses después de la cirugía de reemplazo valvular. Relacionado con el procedimiento, con probable agente hospitalario.
- Válvula protésica intermedia: Aparece entre 2-12 meses después de la cirugía de reemplazo valvular. Imposible determinar si el agente es hospitalario o comunitario.
- Válvula protésica tardía: Aparece más de 12 meses después de la cirugía de reemplazo valvular. No relacionado con el procedimiento, con probable agente comunitario.
Diagnóstico diferencial
- Infección de tejidos blandos.
- Infección del torrente sanguíneo (asociada con catéter vascular).
- ICD o infección del marcapasos.
- Osteomielitis.
- Infección de prótesis articular.
- Meningoencefalitis.
- Neumonía.
- Sepsis.
Seguimiento
Ingreso hospitalario
Todos los pacientes con endocarditis sospechada o diagnosticada deben ser ingresados para tratamiento antibiótico parenteral y tratamiento de seguimiento.
Enfoque terapéutico
Endocarditis infecciosa aguda: Debe ser tratada como una infección grave, requiriendo altas dosis de antibióticos parenterales siempre en asociación, apuntando a las causas probables en terapia empírica y optando por tratamiento específico después de resultados de cultivos y antibiograma. Recopile cultivos y luego inicie la terapia con antibióticos, siempre que sea posible; si el paciente está inestable debido a la endocarditis, los antibióticos se inician al menos después de la recolección de la segunda serie de hemocultivos.
Endocarditis infecciosa subaguda: Recoger cultivos y esperar sus resultados para iniciar antibioticoterapia específica.
Principios de la terapia con antibióticos:
- La monoterapia no es deseable para abordar los factores bactericidas y bacteriostáticos. La gentamicina junto con otros antibióticos puede ayudar con el efecto bactericida, además de reducir el tiempo de tratamiento y tratar patógenos complicados como el enterococo.
- El tratamiento antibiótico de la endocarditis debe guiarse por hemocultivos, que son positivos en más del 90% de los casos.
- La mayoría de los pacientes pueden esperar los resultados de los cultivos para iniciar los antibióticos. La antibioticoterapia empírica debe ser individualizada, como en los casos de inestabilidad hemodinámica o endocarditis aguda (fiebre, malestar general, postración, embolia).
- El tiempo de tratamiento debe partir de los hemocultivos negativos; a los pacientes que se someten a cirugía de reemplazo o reparación de válvula no se les debe reiniciar el recuento después de la cirugía a menos que se identifique un germen en la válvula extraída. Por lo tanto, el tratamiento debe seguir el perfil de sensibilidad del germen referido.
- El uso de gentamicina en infecciones estafilocócicas ya no está indicado debido a la falta de evidencia de beneficio. Cuando estaba indicado, debía tomarse en una sola dosis diaria, para reducir los efectos nefrotóxicos.
- El tiempo de tratamiento es de unas 4-6 semanas, y las razones para prolongar el tratamiento son la presencia de vegetación, microorganismos resistentes y el uso de fármacos bactericidas de acción lenta, como la vancomicina, por ejemplo.
Tratamiento antibiótico empírico:
- Válvula nativa/comunitaria: Oxacilina + penicilina G, Ampicilina o Cefalosporina + gentamicina.
- Usuarios nosocomiales/sospechosos de MRSA/Usuarios de drogas EV/alérgicos a la penicilina: Vancomicina.
- Válvula protésica: Vancomicina + gentamicina + rifampicina.
Tratamiento antibiótico específico: Duración del tratamiento 4-6 semanas:
- Estreptococos sensibles a la penicilina: Penicilina G o Ceftriaxona.
- Estreptococos de resistencia intermedia a la penicilina: Penicilina G + gentamicina (en las 2 primeras semanas).
- Estreptococos resistentes a la penicilina: Vancomicina + gentamicina.
- Estafilococos sensibles a la meticilina (MSSA): Oxacilina (+ gentamicina durante 3-5 días).
- Estafilococos resistentes a la meticilina (MRSA): Vancomicina o daptomicina.
- Enterococos: Vancomicina + gentamicina.
- Grupo HACEK: Ceftriaxona o Ampicilina + sulbactam.
Indicaciones de Daptomicina en EI: Uso reciente de glucopéptidos, insuficiencia renal y/o uso de fármacos nefrotóxicos asociados, MRSA con CIM para Vancomicina > 1 microgramo/mL, o fracaso del tratamiento con Vancomicina.
Importante: Linezolid, Tigeciclina, Teicoplanina y Sulfametoxazol + Trimetoprim no están indicados para el tratamiento de la endocarditis estafilocócica.
Dispositivos intravasculares: Los dispositivos intravasculares que son la fuente de la infección deben retirarse inmediatamente.
Fístula arteriovenosa: Aunque la infección puede originarse en una fístula arteriovenosa, rara vez es necesario deshacer la fístula. Las pruebas de imagen son útiles para diagnosticar un absceso que necesita ser drenado. La imposibilidad de utilizar temporalmente la fístula debe ser suplida por otra fuente de hemodiálisis, por ejemplo, un catéter venoso central.
Dispositivos cardíacos implantables: Los dispositivos cardíacos deben retirarse por completo en las siguientes situaciones:
- Ecocardiograma transesofágico que demuestra vegetación en la válvula o el mango del dispositivo.
- Bacteriemia de alto grado (dos o más cultivos positivos con al menos 1 hora de diferencia) con estafilococos coagulasa negativos o Cutibacterium.
- Alto grado de bacteriemia sin otra fuente conocida de infección.
- Infección del bolsillo del marcapasos.
- Hemocultivo positivo para S. aureus o Candida .
Colonoscopia: Para pacientes con infección por estreptococos del grupo D (bovis/equinus) o enterococos de origen desconocido, está indicada la colonoscopia, dada la fuerte asociación con el cáncer de colon.
Cuidado con la higiene dental: Todos los problemas dentales deben resolverse mientras se realiza la terapia con antibióticos. Es importante que todos los brotes sean tratados.
Respuesta al tratamiento: Mejoría objetiva y subjetiva del cuadro, resolución de la fiebre en 1 semana y hemocultivo negativo (monitorizar diariamente). El tratamiento generalmente dura de 4 a 6 semanas.
Indicaciones para el tratamiento quirúrgico
La indicación del tratamiento quirúrgico de la endocarditis dependerá del estado clínico del paciente afectado y de su respuesta al tratamiento antibiótico.
Es importante recalcar que, antes de proceder a la cirugía cardíaca, el paciente debe ser evaluado por complicaciones como aneurisma micótico y embolia séptica a otros órganos. Estas complicaciones deben ser resueltas antes de la cirugía cardíaca. No obstante, la cirugía debe realizarse lo antes posible tras su indicación.
Los pacientes con embolia al sistema nervioso central sin sangrado, aunque con mayor riesgo, deben ser intervenidos quirúrgicamente.
Las principales indicaciones son:
- Lesión de la válvula que culmina en hipertrofia de la cámara e insuficiencia cardíaca.
- Pacientes con lesiones complejas, como perforación y destrucción de válvulas, abscesos, fístulas, disfunción o dehiscencia de válvulas protésicas y bloqueo auriculoventricular completo.
- Pacientes con endocarditis con patógenos de difícil tratamiento (hongos, microorganismos multirresistentes).
- Pacientes con infección persistente a pesar de la terapia antibiótica adecuada y exclusión de infección en otros sitios.
- Prevención de embolias en pacientes con grandes vegetaciones (> 10 mm) y eventos embólicos en otros sitios (indicación controvertida).
Después de la cirugía, se debe reiniciar el curso de antibióticos. Si los cultivos de la válvula extirpada son negativos, se debe mantener el plan inicial de duración de la terapia con antibióticos. De lo contrario, se debe iniciar un nuevo ciclo de antibióticos y continuarlo durante 6 a 8 semanas.
Prescripcion hospitalaria
Tratamiento empírico: Válvula nativa y prótesica tardía
Recomendaciones:
- Se considera válvula protésica tardía aquella que fue reemplazada hace 12 meses o más.
- El tratamiento antibiótico de la endocarditis debe guiarse por hemocultivos, que son positivos en más del 90% de los casos.
- La mayoría de los pacientes pueden esperar los resultados de los cultivos para iniciar antibióticos, la antibioterapia empírica debe ser individualizada, como en los casos de inestabilidad hemodinámica o endocarditis aguda (fiebre, malestar general, postración, embolia).
- El tiempo de tratamiento debe partir de los hemocultivos negativos; a los pacientes que se someten a cirugía de reparación o reemplazo de válvula no se les debe reiniciar el recuento después de la cirugía a menos que se identifique un germen en la válvula extraída. Por lo tanto, el tratamiento debe seguir el perfil de sensibilidad del germen referido.
Tratamiento farmacológico: Elija uno de los siguientes esquemas a continuación:
Esquema A: Primera linea: Asociación:
- Oxacilina 2 g EV cada 4 horas durante 6 semanas. +
- Gentamicina 3 mg/kg EV/IM cada 24 horas durante 2 semanas. +
- Betalactámico o Cefalosporina.
Opciones de betalactámicos o cefalosporinas:
- Penicilina G cristalina 24 millones de unidades/día, repartidas en cada 4 horas, durante 6 semanas.
- Ampicilina 2 g EV cada 4 horas durante 6 semanas.
- Ceftriaxona 2 g EV cada 24 horas durante 6 semanas.
Esquema B: Asociación:
- Vancomicina 15-20 mg/kg EV cada 12 horas durante 6 semanas. +
- Gentamicina 3 mg/kg EV/IM cada 24 horas durante 2 semanas. +
- Betalactámico o Cefalosporina.
Opciones de betalactámicos o cefalosporinas:
- Penicilina G cristalina 24 millones de unidades/día, repartidas en cada 4 horas, durante 6 semanas.
- Ampicilina 2 g IV cada 4 horas durante 6 semanas.
- Ceftriaxona 2 g IV cada 24 horas durante 6 semanas.
Esquema C: Asociación:
- Daptomicina 6 mg/kg EV cada 24 horas durante 6 semanas. +
- Gentamicina 3mg/kg EV/IM 24/24 horas durante 2 semanas. +
- Betalactámico o Cefalosporina.
Opciones de betalactámicos o cefalosporinas:
- Penicilina G cristalina 24 millones de unidades/día, repartidas en 4/4 horas, durante 6 semanas.
- Ampicilina 2 g IV cada 4 horas durante 6 semanas.
- Ceftriaxona 2 g IV cada 24 horas durante 6 semanas.
Tratamiento empírico: Válvula protésica temprana
Consideraciones:
- Se considera válvula protésica temprana aquella que se reemplazó hace menos de 12 meses.
- El tratamiento antibiótico de la endocarditis debe guiarse por hemocultivos, que son positivos en más del 90% de los casos.
- La mayoría de los pacientes pueden esperar los resultados de los cultivos para iniciar antibióticos, la antibioterapia empírica debe ser individualizada, como en los casos de inestabilidad hemodinámica o endocarditis aguda (fiebre, malestar general, postración, embolia).
- El tiempo de tratamiento debe partir de los hemocultivos negativos; a los pacientes que se someten a cirugía de reemplazo o reparación de válvula no se les debe reiniciar el recuento después de la cirugía a menos que se identifique un germen en la válvula extraída. Por lo tanto, el tratamiento debe seguir el perfil de sensibilidad del germen referido.
Tratamiento farmacológico: Elija uno de los siguientes esquemas: a continuación.
Esquema A: Primera línea: Asociación:
- Vancomicina 30 mg/kg EV cada 12 horas durante 6 semanas. +
- Gentamicina 3 mg/kg EV/IM cada 24 horas durante 2 semanas. +
- Rifampicina 300 mg VO/EV cada 8 a 6 horas durante 6 semanas (comenzar después de 3-5 días de tratamiento).
Esquema B: Asociación:
- Daptomicina 6 mg/kg EV cada 24 horas durante 6 semanas. +
- Gentamicina 3 mg/kg EV/IM cada 24 horas durante 2 semanas. +
- Rifampicina 300 mg VO/EV cada 8 a 6 horas durante 6 semanas (comenzar después de 3-5 días de tratamiento).
(Ver – Pericarditis aguda)
Referencias bibliográficas
Pericàs JM, et al. Prospective Cohort Study of Infective Endocarditis in People Who Inject Drugs. J Am Coll Cardiol. 2021;77:544.
Bläckberg A, et al. Infective endocarditis caused by HACEK group bacteria-a registry-based comparative study. Eur J Clin Microbiol Infect Dis 2021;40:1919.
Berge A, et al. Epidemiology, bacteriology, and clinical characteristics of HACEK bacteremia and endocarditis: a population-based retrospective study. Eur J Clin Microbiol Infect Dis. 2021;40:525.
Kreuzpaintner G, et al. Increased risk of bacterial endocarditis in inflammatory bowel disease. Am J Med. 1992;92:391.
Iversen K, et al. Partial Oral versus Intravenous Antibiotic Treatment of Endocarditis. N Engl J Med. 2019;380:415.
Writing Committee Members, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2021;77:e25.
Cahill TJ, et al. Challenges in Infective Endocarditis. J Am Coll Cardiol. 2017;69(3):325-344.
Pant S, et al. Trends in infective endocarditis incidence, microbiology, and valve replacement in the United States from 2000 to 2011. J Am Coll Cardiol. 2015;65:2070.
Ambrosioni J, et al. The Changing Epidemiology of Infective Endocarditis in the Twenty-First Century. Curr Infect Dis Rep. 2017;19:21.
Habib G, et al. 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Eur Heart J. 2015.
Holland TL, Arnold C, Fowler VG Jr. Clinical management of Staphylococcus aureus bacteremia: a review. JAMA. 2014.
Baddour LM, et al. Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for Healthcare Professionals From the American Heart Association. Circulation. 2015;132:1435.
Tleyjeh IM, et al. Conclusion about the association between valve surgery and mortality in an infective endocarditis cohort changed after adjusting for survivor bias. J Clin Epidemiol. 2010;63:130.
Nishimura RA, et al. 2017 AHA/ACC Focused Update of the 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol. 2017.
Nishimura RA, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2014;63:e57.
Wang A, Gaca JG, Chu VH. Management Considerations in Infective Endocarditis: A Review. JAMA. 2018; 320:72.
Sugerencias y comentarios al correo: contacto@galenbook.com

