Actualizado 13 junio 2023
Definición
Infección ósea bacteriana o fúngica resultante de diferentes procesos patológicos y de presentación variable. Puede ser monomicrobiano o polimicrobiano.
Fisiopatología
Tiene diferentes etiologías con distintos procesos fisiopatológicos:
- Hematógenas: Resulta de procedimientos:
- Bacteriemia y depósito de bacterias en el hueso.
- Reacción inflamatoria local y formación de abscesos.
- El crecimiento del absceso conduce a un aumento de la presión intramedular y a la isquemia cortical.
- Necrosis cortical y extravasación de material purulento al espacio subperióstico. Formación de abscesos subperiósticos.
- Secuestro y cronificación ósea.
- Exógena (no hematógena): Propagación local a través de infecciones de tejidos blandos y articulares adyacentes al tejido óseo o por inoculación directa como resultado de traumatismo, mordedura o cirugía.
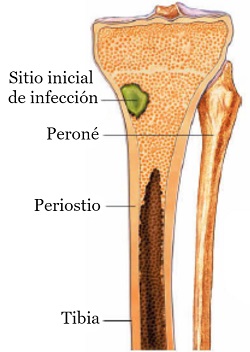
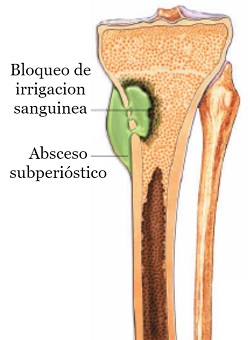
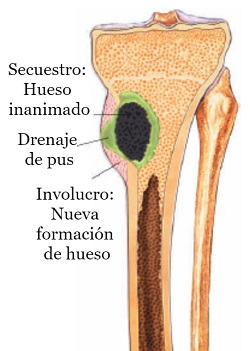
Se clasifica como aguda cuando su manifestación ocurre durante días a algunas semanas, y como crónico cuando los síntomas duran meses a años.
La osteomielitis crónica se asocia comúnmente con la presencia de fragmentos óseos en proceso de necrosis separados del hueso viable, con evidencia de tracto sinusal. Las condiciones asociadas al post-operatorio de osteosíntesis de las fracturas se clasifican siempre como crónicas, independientemente del tiempo transcurrido desde la cirugía.
Etiología
Los posibles patógenos ya descritos asociados con la osteomielitis incluyen Staphylococcus aureus (el más común), estafilococos coagulasa negativos, enterococos, estreptococos, bacilos gramnegativos, incluidos especialmente Pseudomonas aeruginosa y Serratia marcescens, y Aspergillus spp. Otros patógenos menos comunes son Mycobacterium tuberculosis, Candida spp, Bartonella henselae, Brucella melitensis, Coccidioides immitis y Cutibacterium (Propionibacterium) acnes.
Presentación clínica
Osteomielitis hematógena aguda
Epidemiología:
- Es el tipo de infección ósea más común y, en general, monomicrobiana.
- La incidencia ha disminuido significativamente en las últimas décadas debido a la mejora de las condiciones sanitarias e higiénicas.
- Más común en niños.
- Raro después del cierre fisario, generalmente ocurre en pacientes inmunocomprometidos y afecta el cuerpo vertebral.
- Distribución bimodal en niños: < 2 años y entre 8 y 12 años.
- Más común en hombres, en todos los grupos de edad.
- En los niños, suele afectar la región metafisaria de los huesos largos.
- Puede asociarse a trauma local, desnutrición, inmunosupresión y enfermedades crónicas.
- Las formas más comunes son: Vertebral, esternoclavicular, pélvica, en huesos largos y/o enfisematosa.
Cuadro clínico (los síntomas pueden variar significativamente):
- Fiebre, que puede o no estar presente.
- El dolor y la sensibilidad están frecuentemente asociados o no a la movilización.
- Es común el dolor con la presión de los dedos metafisarios.
- El edema local y la hiperemia pueden ser significativos e indicativos de un proceso infeccioso en curso.
Osteomielitis subaguda
Comienzo insidioso y síntomas más leves. El diagnóstico generalmente se realiza dos semanas después del inicio de los síntomas. Se cree que ocurre por la combinación de un germen de baja virulencia con una respuesta inmunitaria significativa del huésped. Es responsable de un tercio de las infecciones óseas primarias.
Cuadro clínico:
- Fiebre ausente o apenas baja.
- El dolor de leve a moderado suele ser el único síntoma.
- Por lo general, leucograma normal.
- VHS aumentado en sólo el 50% de los casos.
- Los hemocultivos casi siempre son negativos.
- Aspirado óseo positivo en solo el 60% de los casos.
- Radiografías y gammagrafías positivas en la mayoría de los casos.
Osteomielitis crónica
Las úlceras profundas o extensas con fallas en el proceso de cicatrización o fracturas no resueltas sugieren la aparición de osteomielitis crónica.
Se caracteriza por la presencia de hueso necrótico infectado con envoltura de partes blandas comprometida (periostio engrosado y fibrosis muscular y subcutánea). Esta envoltura avascular dificulta la acción de la terapia antibiótica sistémica.
Pueden presentarse signos de flogosis (fiebre, eritema y/o edema), comúnmente asociados a un trayecto fistuloso con drenaje de material infectado, lo que corresponde a un signo patognomónico de la condición crónica. La fiebre no es un signo común.
Las infecciones secundarias son frecuentes. El cultivo del trayecto de la fístula por lo general no coincide con el cultivo óseo.
La osteomielitis crónica también puede estar presente como fracturas que no se resuelven.
Factores de riesgo
Factores sistémicos:
- Insuficiencia renal.
- Desnutrición.
- Insuficiencia hepática.
- Diabetes mellitus.
- Endocarditis.
- Consumo de drogas inyectables.
- Uso de accesos cardiovasculares.
- Hemodiálisis.
- Artritis reumatoide.
- Hipoxia crónica.
- Enfermedades inmunológicas e inmunosupresión.
- Anemia de células falciformes.
- Tabaquismo.
- Neoplasmas malignos.
Factores locales:
- Linfedema crónico.
- Estasis venosa.
- Compromiso vascular periférico.
- Presencia de prótesis.
- Procedimiento invasivo previo (punción lumbar, mielografía, aortografía translumbar, quimionucleolisis, discografía, inyección de esteroides articular o epidural, colocación de catéter epidural).
- Arteritis.
- Fibrosis por radiación.
- Neuropatía.
Marcadores de gravedad:
- Compromiso sistémico.
- Infecciones crónicas.
- Pseudoartrosis infectada.
- Huesped con multiples morbilidades.
- Infección periprotésica.
Complicaciones:
- Fistulización.
- Infección de tejidos blandos adyacentes por contigüidad.
- Abscesos.
- Artritis septica.
- Deformación ósea
- Neoplasia ósea.
- Fractura.
Enfoque diagnóstico
Exámenes de laboratorio de rutina: Hemograma, urea, creatinina, electrolitos, enzimas musculares, VHS y PCR, hemocultivos y biopsia ósea (abierta o percutánea) con estudio histopatológico y microbiológico:
- Cambios principales: Leucocitosis neutrofílica con predominio de formas inmaduras (desviacion a la izquierda) en la osteomielitis aguda; aumento de los marcadores inflamatorios (VHS y PCR).
Estudios de imagen: Osteomielitis hematógena aguda
Radiografias:
- Usualmente normal, y puede presentar solo edema de partes blandas.
- Los hallazgos radiográficos óseos (reacción perióstica, destrucción ósea) comúnmente aparecen de 10 a 12 días después del inicio de la afección.
- Diagnósticos diferenciales radiográficos: Artritis séptica, sarcoma de Ewing, osteosarcoma, AIJ, crisis de células falciformes, enfermedad de Gaucher y fractura por estrés.
Gammagrafía con tecnecio-99m:
- Confirma el diagnóstico en el 90-95% de los pacientes 24-48 horas después del inicio de los síntomas.
- Una gammagrafía negativa excluye el diagnóstico de osteomielitis.
Resonancia magnética (RM):
- Alta sensibilidad (98%) pero baja especificidad (75%).
- Presenta hiposeñal en T1 e hiperseñal en T2.
- Muestra cambios inflamatorios tempranos en la médula ósea y tejidos blandos, además de ser muy útil para la delimitación de abscesos intraóseos o subperiósticos.
Ultrasonografía: Precisión del 60% para el diagnóstico de osteomielitis.
Estudios de imagen: Osteomielitis subaguda y crónica
Radiografías:
- Destrucción cortical y reacción perióstica.
Tomografía computarizada:
- Excelente para definir áreas de secuestro.
Fistulografía:
- Ayuda a localizar los focos de infección.
Gammagrafía:
- Más útil en casos agudos, ya que generalmente no se observan hallazgos radiográficos.
Resonancia magnética:
- Lo mejor para la evaluación de tejidos blandos.
- Puede mostrar un halo de hiperseñal que involucra focos de enfermedad activa ( signo del riñón ) en secuencias potenciadas en T2.
Hemocultivos: Positivos en el 50% de los casos de osteomielitis aguda, principalmente en presencia de signos de infección sistémica, pero raramente positivos en presencia de osteomielitis crónica.
Biopsia ósea (abierta o percutánea):
- Examen gold standard en el diagnóstico de osteomielitis, incluso para determinar el patógeno y la sensibilidad antimicrobiana, orientando el tratamiento antimicrobiano.
- Se deben recolectar fragmentos óseos y enviar material para histopatología y cultivos. El número de fragmentos óseos debe ser ≥ 5 y representativo de las áreas posiblemente afectadas.
- Después de la recolección, el material debe enviarse rápidamente al laboratorio.
Hisopado: No se correlaciona bien con la biopsia ósea (no recomendado).
Criterios diagnósticos
El diagnóstico se confirma por la presencia de signos clínicos sumado al resultado de cultivos óseos recogidos y exámenes radiológicos.
En el caso de una condición hematógena aguda, la etiología puede confirmarse mediante hemocultivos.
Clasificación
Descriptivo
En cuanto a la duración de los síntomas:
- Agudo.
- Subaguda.
- Crónico.
En cuanto al mecanismo de infección:
- Hematógeno.
- Exógeno.
En cuanto a la respuesta del huésped a la infección:
- Piógeno.
- No piógeno.
Roberts-Gledhill (subaguda)
- Tipo IA: Imagen perforada radiotransparente sugestiva de granuloma eosinofílico.
- Tipo IB: Similar, pero con esclerosis; es el clásico absceso de Brodie.
- Tipo II: Lesión metafisaria con pérdida cortical.
- Tipo III: Lesión diafisaria con reacción cortical excesiva; similar al osteoma osteoide.
- Tipo IV: Lesión en capas de piel de cebolla asociada del hueso subperióstico similar al sarcoma de Ewing.
- Tipo V: Imagen radiolúcida concéntrica epifisaria.
- Tipo VI: Lesión del cuerpo vertebral.
Cierny-Mader (Crónica)
- Tipo 1: Medular.
- Tipo 2: Superficial.
- Tipo 3: Localizado.
- Tipo 4: Difuso.
- Huesped A: Normal.
- Huésped B: Salud comprometida local o sistémicamente.
- Huesped C: Cuando los resultados del tratamiento son potencialmente más perjudiciales que la afección que se presenta.
Diagnóstico diferencial
- Artropatía de Charcot.
- Infección de tejidos blandos (celulitis, erisipela).
- Bursitis.
- Gota.
- Fractura.
- Malignidad ósea.
- Crisis de oclusión vascular en la anemia de células falciformes.
- Osteonecrosis.
- Enfermedad espinal degenerativa.
- Absceso epidural.
- Herniopatía en la columna vertebral.
- Síndrome SAPHO (sinovitis, acné, pustulosis, hiperostosis y osteítis).
- Síndrome de dolor regional complejo.
Enfoque terapéutico
Antibioticoterapia + considerar el desbridamiento quirúrgico:
- Terapia con antibióticos:
- Debe guiarse por cultivo y antibiograma. Si los cultivos no son accesibles, se debe iniciar terapia antibiótica empírica de amplio espectro (comúnmente glucopéptido, Daptomicina o Linezolid asociado con cefalosporina de tercera o cuarta generación, Carbapenem, Fluoroquinolona o Aztreonam). Debe asociarse al desbridamiento quirúrgico siempre que esté indicado.
- Duración del tratamiento: Normalmente durante seis semanas. En general, el tiempo antimicrobiano debe contarse desde el procedimiento quirúrgico correctivo. Se puede considerar el inicio de tratamiento intravenoso con conversión a terapia oral en función de los resultados microbiológicos. La terapia con antibióticos debe continuarse hasta que el tejido desbridado esté cubierto por tejido blando vascularizado.
- Puede ser útil monitorear la respuesta terapéutica mediante marcadores de laboratorio de inflamación sistémica (VHS y PCR). Si el hueso infectado se ha resecado por completo, la duración del tratamiento puede acortarse.
- Implante ortopédico:
- Ante la presencia de un implante infectado, se debe tomar la decisión entre su mantenimiento o remoción. En el caso de las prótesis de reemplazo articular, las infecciones crónicas se tratan con revisión y reemplazo de las mismas o intento de rescate en caso de infecciones agudas. En fracturas, si se produce consolidación, se debe retirar el implante. Si no hay consolidación, el implante puede ser reemplazado por dispositivos de fijación externa o mantenido junto con el tratamiento de la condición infecciosa, siendo necesario extender el tiempo de cobertura de tres a seis meses.
- Si se mantiene el implante, en algunos pacientes la antibioticoterapia se puede mantener indefinidamente como método supresor. Ante la sospecha de infección por S. aureus y mantenimiento de la prótesis se debe asociar Rifampicina como adyuvante, pero este antimicrobiano sólo debe iniciarse a los cinco a siete días del inicio del esquema principal.
- Infección de tejidos blandos asociada: Si existe una asociación con infección de tejidos blandos adyacentes (celulitis), se debe iniciar tratamiento empírico, preferiblemente después de la recolección de cultivos.
- Complicaciones:
- En ausencia de un tratamiento adecuado, la osteomielitis aguda puede asociarse con discapacidad funcional o complicaciones fatales.
- La infección supurativa puede afectar estructuras contiguas, como articulaciones y tejidos blandos, lo que lleva a la formación de fístulas.
- También pueden ocurrir fracturas patológicas debidas a osteólisis. Aunque es raro, puede ocurrir diseminación hematógena y progresión a sepsis grave, lo que dificulta determinar el sitio primario de infección (torrente sanguíneo o hueso).
- La formación de fístulas puede estar asociada a neoplasias, especialmente en infecciones de larga duración.
- La mayoría de los pacientes con neoplasia tienen antecedentes de intervenciones quirúrgicas repetidas.
- El tumor maligno se caracteriza por una masa en constante crecimiento, con dolor creciente, drenaje maloliente, sangrado o evidencia radiográfica de destrucción ósea.
- La infección recurrente/refractaria, que no responde a la terapia convencional, debe por lo tanto ser evaluado por biopsia para malignidad de múltiples sitios (incluyendo úlcera, fístula y hueso subyacente).
Prescripción hospitalaria
Todas las formas clínicas: Antibioticoterapia empírica
Esquema: Tratamiento empírico con asociación:
- Glucopéptido, Daptomicina o Linezolid durante 6-12 semanas. +
- Cefalosporinas de tercera o cuarta generación, Carbapenemico, Fluoroquinolonas o Aztreonam, por 6-12 semanas.
Opciones de glucopéptidos, daptomicina, linezolid:
- Vancomicina 15-20 mg/kg/dosis (sin exceder 2 g por dosis) IV cada 8/8 a 12/12 horas para cobertura empírica de MRSA.
- Teicoplanina (6-12 mg/kg) 400 mg EV cada 12 horas por 3 dosis (dosis de carga). Luego 400 mg EV/IM cada 24 horas (dosis de mantenimiento).
- Daptomicina 6-10 mg/kg EV cada 24 horas.
- Linezolid 600 mg VO/EV cada 12 horas.
Opciones de cefalosporinas de tercera o cuarta generación, carbapenémicos, fluoroquinolonas, aztreonam:
- Ceftazidima 2 g EV cada 8 horas.
- Ceftriaxona 2 g EV cada 24 horas.
- Cefepima 2 g EV cada 8 horas.
- Meropenem 1-2 g EV cada 8 horas.
- Imipenem 500 mg EV cada 6 horas o 1 g EV cada 8 horas.
- Ciprofloxacino 400 mg EV o 500 mg VO cada 12 horas.
- Levofloxacino 500-750 mg EV o 500 mg VO cada 24 horas.
- Aztreonam 1-2 g EV cada 8 a 12 horas.
Tratamiento adyuvante
1. Agua borizada (2-3 g/100 mL) 2-3% durante 10 minutos, 2-3 veces al día, con gasa o algodón.
2. Permanganato de potasio (1:20.000) en el baño 2 veces al día.
3. Neomicina + bacitracina en crema: Aplicar sobre la zona 1-3 veces al día.
4. Mupirocina en crema en la zona afectada 3 veces al día.
5. Ácido fusídico al 2% crema: Aplicar sobre la zona 2-3 veces al día.
Referencias bibliográficas
Masters EA, Ricciardi BF, Bentley KLM, et al. Skeletal infections: microbial pathogenesis, immunity and clinical management. Nat Rev Microbiol. 2022; 20(7):385-400.
Schmitt SK. Osteomyelitis. Infect Dis Clin North Am. 2017; 31(2):325-38.
Tornetta P, et al. Rockwood & Green Fractures in Adults. 8th ed. Philadelphia: Lippincott Williams & Wilkins, 2014.
Yang J, Yao JL, Wu ZQ, et al. Current opinions on the mechanism, classification, imaging diagnosis and treatment of post-traumatic osteomyelitis. Chin J Traumatol. 2021; 24(6):320-327.
Zhang Y, et al. Adjunctive rifampin therapy for diabetic foot osteomyelitis: A protocol for systematic review and meta-analysis. Medicine (Baltimore). 2020; 99:e20375.
Lázaro-Martínez JL, et al. Antibiotics versus conservative surgery for treating diabetic foot osteomyelitis: a randomized comparative trial. Diabetes Care. 2014; 37:789.
Lew DP, Waldvogel FA. Osteomyelitis. Lancet. 2004; 364:369-379.
Li HK, et al. Oral versus intravenous antibiotics for bone and joint infection. N Engl J Med. 2019; 380:425.
Lima AL, Oliveira PR, Carvalho VC, et al; Diretrizes Panamericanas para el Tratamiento de las Osteomielitis e Infecciones de Tejidos Blandos Group. Recommendations for the treatment of osteomyelitis. Braz J Infect Dis. 2014; 18(5):526-34.
Sugerencias y comentarios al correo: contacto@galenbook.com

