Actualizado 11 agosto 2024
Definición
Neoplasia angioproliferativa causada por el virus herpes tipo 8. También conocida como hiperplasia reactiva multifocal del endotelio vascular.
Fisiopatología
El virus herpes tipo 8 (HHV-8), con sus propiedades oncogénicas, está asociado con la disfunción del sistema inmunológico. Factores ambientales (Hipótesis: Exposición al suelo volcánico, exposición crónica de la piel al hierro o al silicato de aluminio, infección concomitante por un agente parasitario) y predisposición genética también están implicados.
La infección por el virus ocurre a través de la saliva (por contacto cercano), sangre, productos contaminados con sangre, vía sexual, donación de órganos sólidos y, raramente, por transmisión vertical.
Células endoteliales, dendríticas, monocitos, linfocitos B, células epiteliales y fibroblastos son susceptibles a la infección. También puede afectar el sistema nervioso central en pacientes con SIDA.
El virus tiene una fase lítica de corto periodo y una fase latente (predominante) en las células endoteliales.
En la fase lítica, la inflamación crónica (linfocitos B, plasmocitos y monocitos) y la oncogenicidad son promovidas por genes y proteínas virales que activan señales celulares que inducen la proliferación e inmortalización celular.
Inicialmente, se consideraba una respuesta angioproliferativa reactiva al HHV-8; sin embargo, debido a los efectos continuos de los genes virales que interrumpen la apoptosis celular, estimulan citocinas y provocan inflamación local, ahora se considera una verdadera neoplasia de células endoteliales.
Ocurre predominantemente en hombres, ya que los receptores androgénicos desempeñan un papel clave en la oncogénesis, facilitando la replicación lítica. El tratamiento con esteroides masculinos también promueve una mayor expresión de genes líticos en células infectadas.
Etiología
Causado por el virus herpes tipo 8 (HHV-8), un herpesvirus gamma de ADN de doble hebra.
Presentación clínica
Epidemiología:
- Más común en hombres, personas con VIH, población del Mediterráneo (Italia) y judíos asquenazí de Europa del Este.
- En personas con VIH/SIDA, es más frecuente en hombres que tienen sexo con otros hombres, sobre todo en pacientes con alta carga viral y CD4 < 500/mm³ o tras la restauración de la inmunidad.
- Es el segundo tumor más común en pacientes con SIDA después del linfoma no Hodgkin, aunque su incidencia ha disminuido con la terapia antirretroviral.
- En África Subsahariana, tiene menor prevalencia en hombres y es uno de los principales cánceres reportados.
Manifestaciones clínicas:
- Mácula, pápula, placa o tumor indoloro que puede sangrar fácilmente.
- Puede ocurrir en piel, mucosas (oral, genital, ocular), ganglios linfáticos y/o órganos sólidos (estómago, intestino, pulmón e hígado). Rara vez afecta el sistema musculoesquelético, urinario, endocrino, corazón u ojo (más común en párpados y conjuntiva, aunque también puede involucrar órbita y conducto nasolacrimal).
- En la mucosa oral, el paladar duro es el sitio más afectado.
- El compromiso de párpados y conjuntiva puede ser la primera manifestación del VIH/SIDA.
- La localización en el sistema nervioso central es muy rara y se asocia con infección por VIH y enfermedad diseminada.
Variantes documentadas:
- Clásica o esporádica:
- Hombres mayores (>60 años) de ascendencia mediterránea o judíos asquenazí.
- Lesiones cutáneas en miembros inferiores con edema crónico asociado y curso indolente.
- Infrecuente compromiso visceral.
- Tabaquismo como factor protector.
- Endémica:
- Específica de África Subsahariana, con alta seroprevalencia del virus (>40-50%).
- Niños de 4-9 años: Curso agresivo con linfadenopatía generalizada, compromiso mucocutáneo y visceral.
- Hombres mayores de 40 años: Curso indolente con lesión en extremidades inferiores.
- Subtipos: Nodular, florido, infiltrativo y linfadenopático.
- Epidémica:
- Asociada con VIH/SIDA, con compromiso mucocutáneo diseminado y visceral (más común en sistema pulmonar y gastrointestinal). Curso agresivo.
- Definidora de SIDA.
- Iatrogénica:
- En inmunosuprimidos por trasplantes (2-3 años después del procedimiento), corticoterapia crónica, medicamentos biológicos o inmunosupresores, quimioterapia o trasplante de órgano infectado.
Sarcoma de Kaposi no epidémico: Nueva entidad descrita. Ocurre en hombres que tienen sexo con otros hombres, pacientes jóvenes o de mediana edad y sin infección por el VIH, pero también hay correlación entre el conteo de células T CD4 y la razón CD4/CD8 con la gravedad de la enfermedad. Presenta pocas lesiones, rara afectación visceral y un curso indolente. Pocas lesiones, raramente hay compromiso visceral y tiene un curso indolente.
Marcadores de gravedad:
- Ulceración de las lesiones (más común en SIDA).
- Afectación de órganos internos: Tracto gastrointestinal, ganglios linfáticos, pulmones, etc.
Examen físico:
- Examen físico completo con atención a linfadenopatías y mucosa oral.
- Lesiones eritematosas o violáceas (mácula, pápula, placa o tumor) que no blanquean a la presión.
- Progresión a necrosis central y ulceración.
- Multifocalidad y confluencia de lesiones.
- Posible linfedema asociado.
Dermatoscopia:
- Patrón homogéneo, multicolor en una misma lesión (apariencia de arco iris), áreas blanquecinas sin estructura, escamas, collarete descamativo y estructuras vasculares.
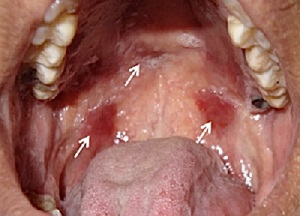
Lesiones maculo-eritematosas erosionadas son zonas hemorrágicas en su superficie, localizadas en paladar blando.
Enfoque diagnóstico
El diagnóstico es clínico y se confirma mediante la biopsia de una de las lesiones.
El análisis histopatológico no distingue la forma clínica, y los hallazgos varían según la etapa de la lesión:
- Etapa de mácula: Proliferación dérmica superficial de pequeños vasos, delicados y angulados, rodeados por un infiltrado de linfocitos y plasmocitos.
- Etapa de placa y nódulos: La proliferación vascular se extiende hacia la dermis profunda, acompañada de proliferación de células fusiformes (que expresan marcadores de células endoteliales), con espacios vasculares en forma de hendiduras, revestidos por células endoteliales atípicas y ocupados por eritrocitos y depósitos de hemosiderina. Puede implicar y/o disecar haces de colágeno. Es posible encontrar el “signo del promontorio” (hernia de un vaso dentro de otro vaso sanguíneo), que es característico, aunque no patognomónico de la enfermedad.
La inmunohistoquímica para detectar el antígeno nuclear asociado a la latencia (LANA-1) del HHV-8 puede ser útil para el diagnóstico, pero requiere un laboratorio especializado. Otros marcadores incluyen: CD34, CD31, ERG, D2-40/podoplanina, PROX1, entre otros.
La detección sérica por serología o PCR del HHV-8 no ha demostrado ser útil.
Exámenes de rutina: Una vez confirmado el diagnóstico, se debe investigar o descartar el compromiso sistémico mediante:
- Anamnesis dirigida.
- Examen físico completo.
- Exámenes de imagen:
- Radiografía de tórax o tomografía computarizada de tórax.
- Ultrasonido abdominal total o tomografía computarizada de abdomen y pelvis.
- Broncoscopia, endoscopia digestiva alta y colonoscopia (si es necesario).
Considerar realizar una prueba de anticuerpos anti-VIH si hay sospecha de SIDA.
Diagnóstico diferencial
- Angiosarcoma bien diferenciado.
- Pseudossarcoma de Kaposi.
- Angiomatosis bacilar.
- Linfoma cutáneo.
- Sífilis.
- Eritema elevatum diutinum.
Complicaciones
Linfedema y estasis linfática crónica.
El sarcoma de Kaposi musculoesquelético con lesión ulcerada puede involucrar el hueso subyacente, generando un efecto osteolítico.
Abordaje terapéutico
El tratamiento depende de la extensión de la enfermedad, si está localizada o diseminada, su evolución, el estado inmunovirológico y las comorbilidades del paciente.
Sarcoma de Kaposi epidémico:
En pacientes con VIH/SIDA aún sin tratamiento, es altamente recomendado el inicio de la terapia antirretroviral (TARV), logrando altos índices de involución de las lesiones tras comenzar el tratamiento. Sin embargo, puede ocurrir el síndrome inflamatorio de reconstitución inmune (IRIS), con un empeoramiento clínico paradójico del sarcoma de Kaposi preexistente o, en raras ocasiones, revelando un sarcoma de Kaposi no diagnosticado previamente, especialmente durante los primeros seis meses de tratamiento. En estos casos, se indica continuar con la terapia antirretroviral, pudiendo añadirse quimioterapia en casos rápidamente progresivos, muy sintomáticos, con afectación visceral o linfedema. Se debe evitar el uso de corticoides, ya que pueden agravar las lesiones.
Sarcoma de Kaposi iatrogénico:
Evaluar el riesgo-beneficio de suspender los inmunosupresores. Los estudios han demostrado que una reducción del 50% en la dosis de inmunosupresores puede resultar en la involución de las lesiones.
Otras opciones de tratamiento:
- Extirpación quirúrgica: Opción para cuadros localizados con una o pocas lesiones pequeñas, superficiales y sin compromiso sistémico. Tiene un alto riesgo de recurrencia.
- Crioterapia (tiempo de congelación necesario para generar ulceración superficial de la epidermis), láser de CO2 y terapia fotodinámica: También indicados para lesiones localizadas, pequeñas y superficiales.
- Radioterapia: Indicada para presentaciones multifocales restringidas a una o dos regiones, o para sarcoma de Kaposi clásico o iatrogénico en el que no se puede suspender la inmunosupresión.
- Quimioterapia sistémica: Indicada en casos rápidamente progresivos o con compromiso sistémico (órganos internos).
- Ejemplos: Doxorrubicina liposomal pegilada, daunorrubicina liposomal, paclitaxel, vincristina + bleomicina, taxanos, interferón α, interferón pegilado, imatinib.
- Inmunoterapia: Opciones en estudio para casos que no responden a las demás terapias.
- Ejemplos: Ipilimumab, nivolumab, pembrolizumab y atezolizumab.
Referencias bibliográficas
Hoffmann C, Sabranski M, Esser S. HIV-Associated Kaposi’s Sarcoma. Oncol Res Treat. 2017; 40(3):94-98.
Bolognia JL, Jorizzo JL, Rapini RP, et al. Dermatology. 2nd ed. St. Louis: Mosby-Elsevier, 2008.
Zeinaty PE, Lebbé C, Delyon J. Endemic Kaposi’s Sarcoma. Cancers (Basel). 2023; 15(3):872.
Rusu-Zota G, Manole OM, Galeș C, et al. Kaposi Sarcoma, the Trifecta of Pathogenic Mechanisms. Diagnostics (Basel). 2022; 12(5):1242.
Grabar S, Costagliola D. Epidemiology of Kaposi’s Sarcoma. Cancers (Basel). 2021; 13(22):5692.
Sugerencias y comentarios al correo: contacto@galenbook.com

